T.IV - UTILISATIONS DES GAZ PARFAITS
Notion de réversibilité
• On appelle “transformation réversible” un
changement d’état thermodynamique pendant lequel le système reste
en quasi-équilibre. Les conditions sont alors quasi-identiques à
celles de la transformation inverse.
Les transformations avec frottements, hystérésis, etc... sont
irréversibles.
☞ remarque : un changement d’état n’est produit qu’en créant un
déséquilibre (la transformation réversible n’est qu’une limite
théorique) ; en pratique on considère des transformations “quasi
réversibles” (proches de la limite).
☞ remarque : il est nécessaire, mais non suffisant qu’une
transformation soit “quasi statique” pour être quasi réversible :
une lente fuite d’une bouteille de gaz est irréversible (le gaz ne
peut pas ainsi rentrer dans la bouteille ! ).
Détentes irréversibles et lois de Joule
Loi de Joule/Gay-Lussac
• La première loi de Joule pour les gaz
(Joule/Gay-Lussac) exprime que l'énergie interne ne dépend que de
la température :
.
En particulier, pour un gaz parfait :
.
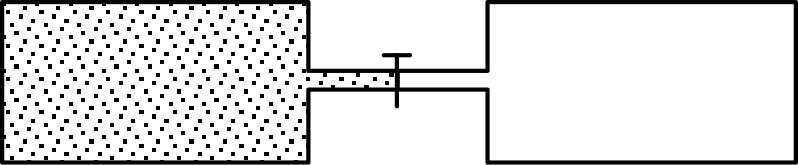
• Cette loi peut être testée avec un assemblage de deux récipients à
parois rigides et adiabatiques, reliés par un tube muni d'un
robinet.
Initialement : le robinet est fermé, le premier récipient est rempli
d'un gaz à la température
, le second
récipient est “vide” (pression négligeable).
On ouvre alors le robinet : le gaz se répartit dans le volume total
disponible et, après une très courte durée nécessaire pour
équilibrer la pression, on mesure la variation de température
du gaz.
• Mécaniquement :
(le gaz se déplace mais il est à nouveau immobile à la fin)
et
(
à la limite du vide où le volume varie) ; d'après l'isolation
thermique :
; donc
.
Or, pour un gaz parfait, on mesure
donc
; ainsi
ne dépend pas
de
.
◊ remarque : l’expérience est délicate car il faut s’assurer que les
transferts d’énergie avec les récipients sont négligeables.
Loi de Joule/Thomson (ou Joule/Kelvin)
• La deuxième loi de Joule pour les gaz
(Joule/Thomson) exprime que l'enthalpie ne dépend que de la
température :
.
En particulier, pour un gaz parfait :
.
• Cette loi peut être testée avec un assemblage de deux récipients à
parois rigides et adiabatiques, reliés par une paroi poreuse. Les
volumes sont réglables par des pistons adiabatiques.
Le récipient de gauche est rempli de gaz à température
et son
piston est manipulé de façon à imposer une pression
constante ;
le second récipient est de même à une pression
constante.
On laisse s'établir un écoulement permanent, assez lent pour pouvoir
négliger l’énergie cinétique macroscopique en comparaison de
l’énergie interne (soit
),
puis on mesure la variation de température
du gaz.
• Mécaniquement :
et
(isolation thermique) ; donc
.
Or, pour un gaz parfait, on mesure
donc
; ainsi
ne dépend pas
de
.
◊ remarque : pour un gaz parfait, il n’y a pas de
“frottement” dans la paroi poreuse ; le fait que les trous soient
petits et que la probabilité de passage des molécules soit faible
suffit à “freiner” cette traversée.
◊ remarque : si l’écoulement est tel que la variation d’énergie
mécanique n’est pas négligeable, on obtient
et la température varie.
Compressions/détentes quasi-réversibles
Compression isotherme quasi-réversible
• Soit un gaz maintenu à température constante
par un thermostat ; on considère une compression isotherme
quasi-réversible : assez lente pour maintenir la température (
s'équilibre
vite, mais
s'équilibre
lentement).
La loi caractéristique est :
(quantité constante à
constante).
• Le travail fourni au système est :
;
c'est un travail moteur pour une compression, résistant pour une
détente.
◊ remarque : on peut aussi écrire :
ce qui est cohérent avec le calcul précédent
puisque
.
• La chaleur fournie au système (par le thermostat) lors de la
transformation découle de la première loi de Joule :
à température constante, c'est-à-dire :
. Le système cède de la chaleur pour une compression au sens
strict, il reçoit de la chaleur pour une détente.
Compression adiabatique quasi-réversible
• Soit un gaz isolé thermiquement ; on considère
une compression adiabatique quasi-réversible : assez lente pour
permettre à la pression de s'équilibrer (ici la contrainte est
nettement moins importante que pour le cas isotherme).
La loi caractéristique d'une telle transformation peut se déduire
de :
,
qui peut s’écrire :
,
c'est-à-dire :
.
La loi des gaz parfaits
impose de plus :
. En éliminant
et avec
:
on obtient :
dont
l'intégration donne la loi d'évolution :
(loi de Laplace).
• D'après la loi des gaz parfaits, la loi de Laplace (entre
et
) impose
aussi des relations équivalentes entre
et
, ou entre
et
.
Pour l'air (
)
comprimé d'un rapport
dans une pompe de bicyclette :
(
) donne
(
).
• Le travail fourni au système lors de la transformation peut
s’écrire :
;
mais plus simplement
donne
directement :
.
C'est un travail moteur pour une compression (d'où un échauffement)
et un travail résistant pour une détente (d'où un refroidissement).
◊ remarque : ce raisonnement se généralise au cas “polytropique”
correspondant à la proportionnalité
.
Calorimétrie et propriétés thermoélastiques
• Les coefficients calorimétriques ne sont pas indépendants des
propriétés thermoélastiques. Considérons par exemple les
coefficients de compressibilité isotherme :
et adiabatique :
.
Dans un diagramme de Clapeyron (en un point commun aux deux
courbes) :
- la pente de l’isotherme
est
;
- la pente de l’adiabatique
est
.
Par comparaison :
(relation de Reech).
• D'autres grandeurs usuelles dépendent du coefficient , par exemple
la vitesse de propagation du son dans les gaz :
où
est la masse
volumique et
la masse
molaire.
📖 exercices n° I, II, III, IV, V et VI.
Cycle moteur et cycle de Carnot
Notion de cycle moteur
• Une transformation thermodynamique peut “changer” de la chaleur en
travail (par exemple la dilatation causée par chauffage…)
; mais pour effectuer ceci en grande quantité, la seule
méthode efficace est utiliser une suite de transformations
“cyclique” (dont l’état final est identique à l’état initial).
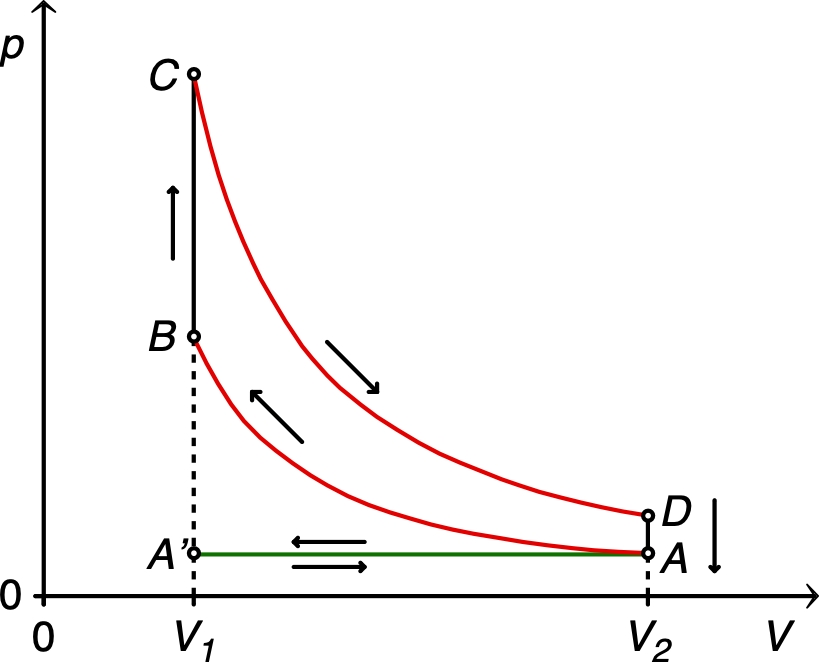
• Le cycle moteur ci-contre, décrit le
fonctionnement d'un moteur à explosion à quatre temps.
Le premier temps (admission) correspond à l'entrée du gaz (
) ;
cette étape ne participe que de façon négligeable aux
transfert thermiques ; elle ne participe pas au travail car
elle est compensée par le dernier temps. |
|
|
Le deuxième temps (compression) correspond en première approximation
à une compression adiabatique quasi-statique (
) ; cette
étape est assez “lente” pour que la pression s'équilibre (c'est
quasi-instantané) mais trop rapide pour qu'un transfert de chaleur
puisse avoir lieu.
Entre le deuxième et le troisième temps, “l’explosion” correspond en
première approximation à une augmentation de pression “isochore” (
, à volume
constant) ; le gaz est renouvelé à chaque cycle, mais cela est
équivalent à ce qu'on pourrait obtenir en conservant le même gaz et
en lui transférant à chaque cycle, depuis l'extérieur, l'équivalent
en chaleur de l’énergie dégagée par la combustion.
Le troisième temps (détente) correspond en première approximation à
une détente adiabatique quasi-statique (
) ; analogue
au deuxième temps.
Le quatrième temps (échappement) peut être en première approximation
décomposé en deux étapes : une diminution de pression isochore (
) suivie
d'une éjection du gaz à pression constante (
) ; le gaz
est renouvelé à chaque cycle, mais cela est équivalent à ce qu'on
pourrait obtenir en conservant le même gaz et en lui prenant à
chaque cycle, depuis l'extérieur, l'équivalent en chaleur de
l'énergie emportée par le gaz qui s'échappe.
Par compensation de (
) et (
), le cycle
équivaut à (
).
◊ remarque : le graphique d'un cycle moteur (
)
est parcouru dans le sens “horaire”.
• La chaleur “reçue” lors de l'explosion s'écrit :
si on néglige les
variations de
. De même,
la chaleur “cédée” lors de l'échappement peut s'écrire :
(cette chaleur peut
être considérée comme “perdue”).
Lors d’un cycle, le travail
fourni
par le moteur doit vérifier la relation :
; le rendement (thermodynamique) du moteur est donc
:
.
Compte tenu de la loi de Laplace pour les adiabatiques quasi
réversibles :
; par suite :
.
Dans les moteurs usuels :
et
; ainsi :
(mais ce calcul simplifié est trop optimiste ; le cycle réel
correspond à
).
◊ remarque : puisque le rendement augmente en fonction du taux de
compression
, les motoristes augmentent la résistance des carburants à la
compression (indice d'octane) pour augmenter
et améliorer le rendement.
◊ remarque : le second principe de la thermodynamique montre qu'il
est possible de réduire la perte de chaleur correspondant à
, mais pas
de l'éliminer : le cycle “idéal” correspond au “cycle de Carnot”.
Cas “idéal” du cycle de Carnot-Clausius
• On dit qu'un système à fonctionnement cyclique
effectue un “cycle de Carnot” lorsqu'il n'échange de la chaleur
qu'avec deux sources et de façon réversible. Cela correspond au
rendement maximum.
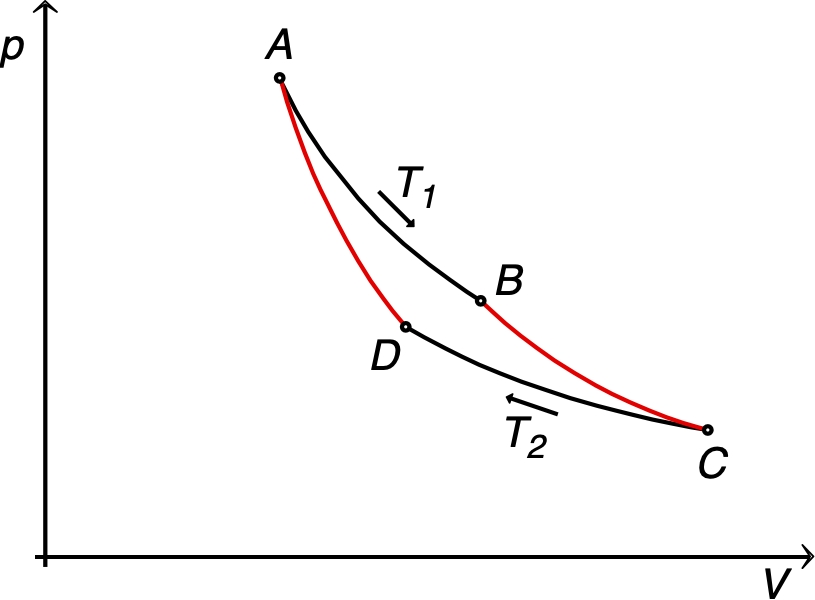
On obtient un cycle de Carnot pour un gaz
parfait en raccordant deux isothermes et deux adiabatiques.
☞ remarque : dans un diagramme de Clapeyron, le cycle est
très “aplati” ; pour plus de lisibilité, on utilise
ici
(maximum possible). |
|
|
Les quantités de chaleur reçues lors des transformations isothermes
(
) et (
) sont
:
et
.
Mais compte tenu de la loi de Laplace pour les adiabatiques (
) et (
) :
; donc :
(relation de
Carnot-Clausius).
Le rendement est donc :
.
◊ remarque : dans ce cas c'est taux d'échauffement
qu'il est souhaitable d'augmenter pour améliorer le rendement.
📖 exercices n° VII, VIII et IX.