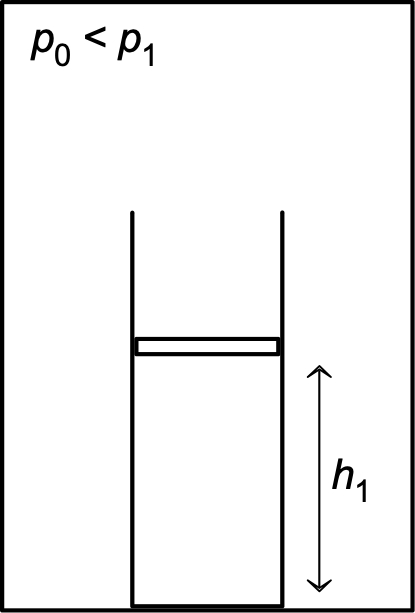
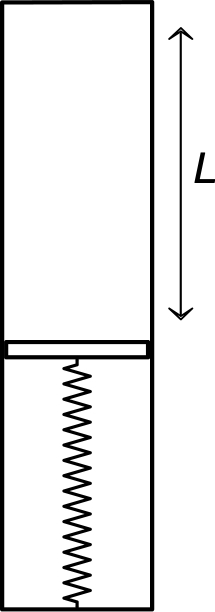
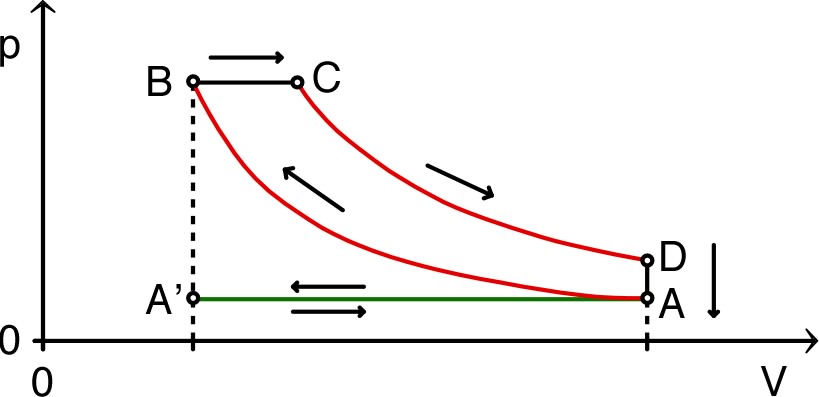
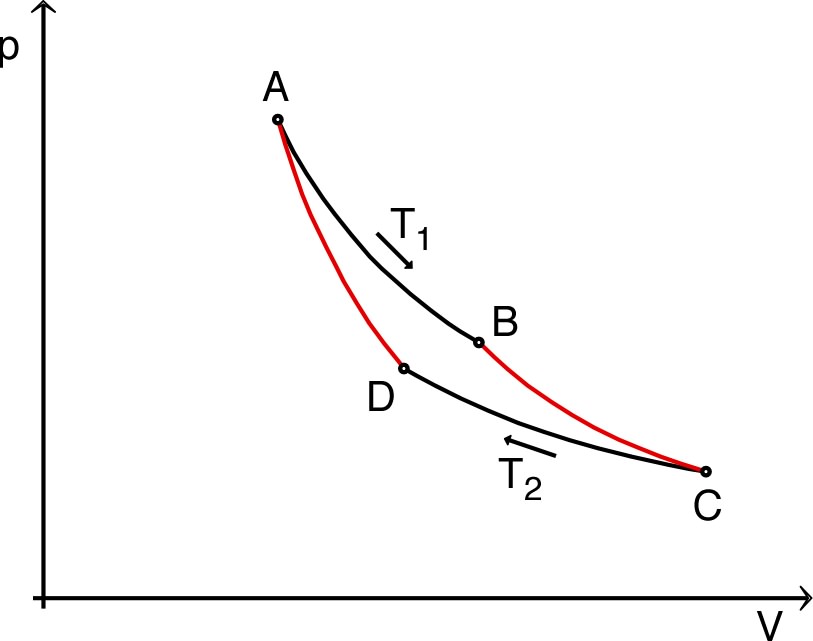
• Le cylindre est placé dans une enceinte dépressurisée, contenant de l'air maintenu à la pression ; la surpression du gaz intérieur au cylindre est équilibrée par un piston pesant, de masse , dont le frottement sur les parois du cylindre est en première approximation négligeable. La température initiale du gaz est .
1. • On écarte légèrement le piston de sa position d'équilibre ; exprimer la période des petites oscillations autour de l'équilibre.