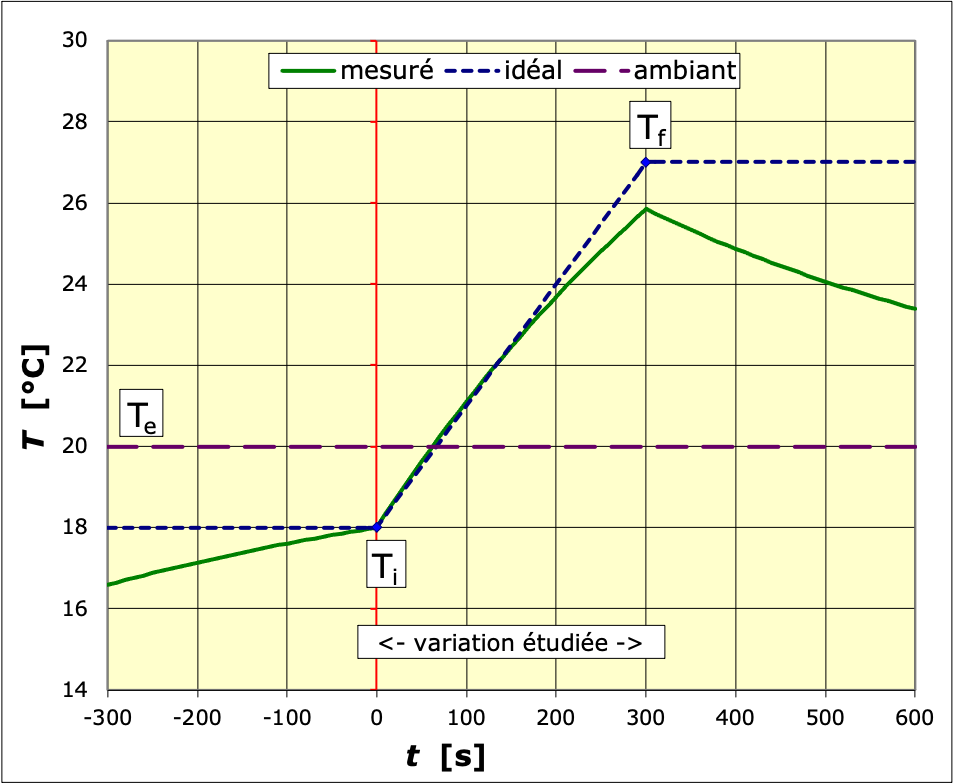
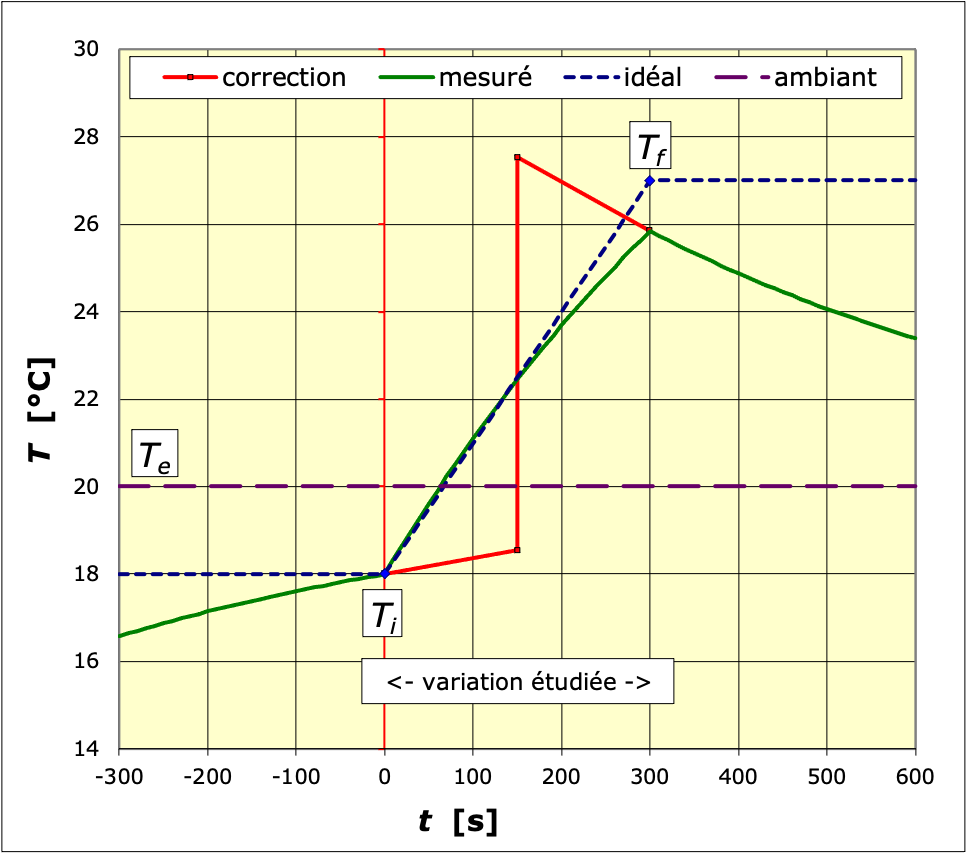
• Pour un calorimètre contenant une masse
d’eau, tracer la variation de température en fonction du
temps, lors d’un échauffement à tension et courant
connus (par exemple
à
et
à
pour
).
En déduire la capacité thermique du système.
◊ remarque : agiter pendant la manipulation, pour
“uniformiser” la température (mais en isolant la partie de
l’agitateur au contact des doigts).
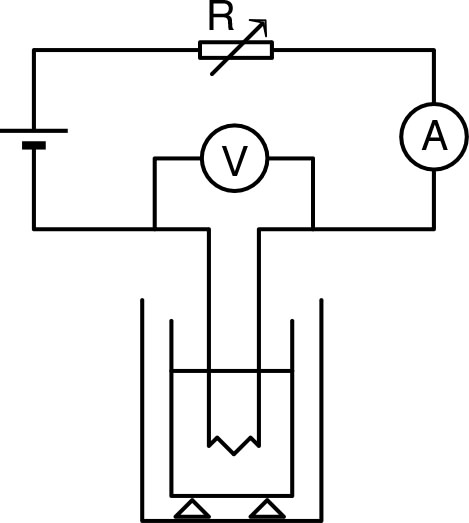
◊ remarque : la valeur de
doit être assez grande pour que la résistance trempe dans
l'eau (faute de quoi, non seulement le chauffage est
inefficace, mais la résistance risque d'être endommagée
! ), mais asse petite pour que l'échauffement ne soit ni
trop faible, ni trop lent (
entre
et
est souvent acceptable, mais cela dépend du calorimètre
utilisé). |
|
|