MESURE D’UNE CAPACITÉ THERMIQUE - corrigé du TP
Correction des transferts de chaleur parasites
• On considère qu'en bonne approximation les transferts parasites
avec l’extérieur sont décrits par un “flux thermique” de la forme
:
où
est la
température extérieure.
• Si la température varie de façon affine :
(où la notation simplifiée
désigne en
fait
), le
transfert de chaleur parasite correspond à :
.
Mais par ailleurs
donc :
.
En outre, l'expression du flux
étant
affine :
;
.
• Le bilan thermodynamique avec correction peut s'écrire :
; par linéarité des équations, on peut le décomposer en
deux étapes, la première correspondant au cas idéal
ensuite seulement suivie d'une perturbation
. La variation correspondante de la température est alors
telle
que
; ainsi
(cela n'est qu'approximatif car les flux des fuites thermiques
dépendent de la température et celle-ci ne varierait pas
linérairement dans un tel processus, mais l'écart n'est que du
second ordre).
◊ remarque : si la variation de
est
effectivement à peu près affine pour le chauffage électrique,
l'approximation est plus grossière pour la méthode des mélanges.
Manipulation
Capacité thermique de l’eau et méthode du chauffage électrique
• On réalise le montage avec une résistance chauffante
; la résistance dépend un peu de la température et il importe
surtout de mesurer la tension
et le courant
.
Le calorimètre et les autres parties d'aluminium ont une masse
; on y ajoute l'eau et on repèse pour connaître par
différence la masse d’eau
.
◊ remarque : les températures sont ici mesurées avec des
thermomètres de haute précision.
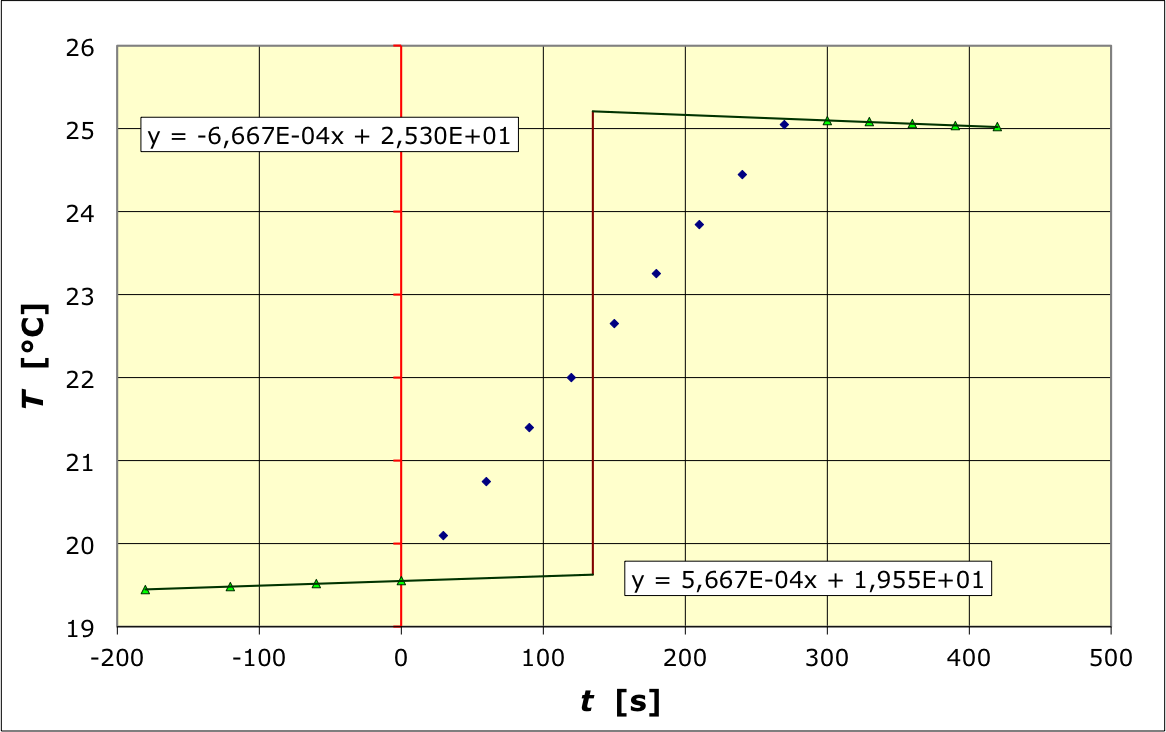
• Pour corriger les fuites thermiques, on ajuste des droites sur les
mesures avant et après chauffage ; leur prolongement jusqu'au milieu
de la durée du chauffage donne une estimation de l'effet de la
puissance moyenne des fuites (cela revient à calculer quelles
seraient les températures aux limites si le travail électrique
avait été
fourni instantanément, donc sans fuite).
On obtient une variation
en une durée
; la variation corrigée des fuites est
donc la correction est pratiquement négligeable (inférieure
aux incertitudes).
◊ remarque : on obtient assez généralement une correction
négligeable en procédant symétriquement par rapport à la
température extérieure, ce qui peut se faire en refroidissant
préalablement un peu le dispositif (en le posant sur des glaçons).
• Le travail électrique est
; la capacité thermique de l'aluminium est
avec une capacité thermique massique
(d'après
les tables de données) donc
; la capacité thermique de l'eau est
et
sa capacité thermique massique est
.
Le résultat est correct mais peu précis avec un seul résultat
d'expérience (très peu d'étudiants parviennent à faire plusieurs
mesures ; l'efficacité de l'organisation inter-groupes est
insuffisante).
Capacité thermique des métaux et méthode des mélanges
• On prépare un bloc de fer de masse
à une température
(dans un bain d’eau chaude à température connue, c'est
toutefois la principale cause d'incertitude). On prépare un
calorimètre (plus l'agitateur) en aluminium de masse
contenant une masse
d’eau (on pèse le calorimètre pendant le remplissage, ce qui
permet de contrôler la masse d'eau par différence).
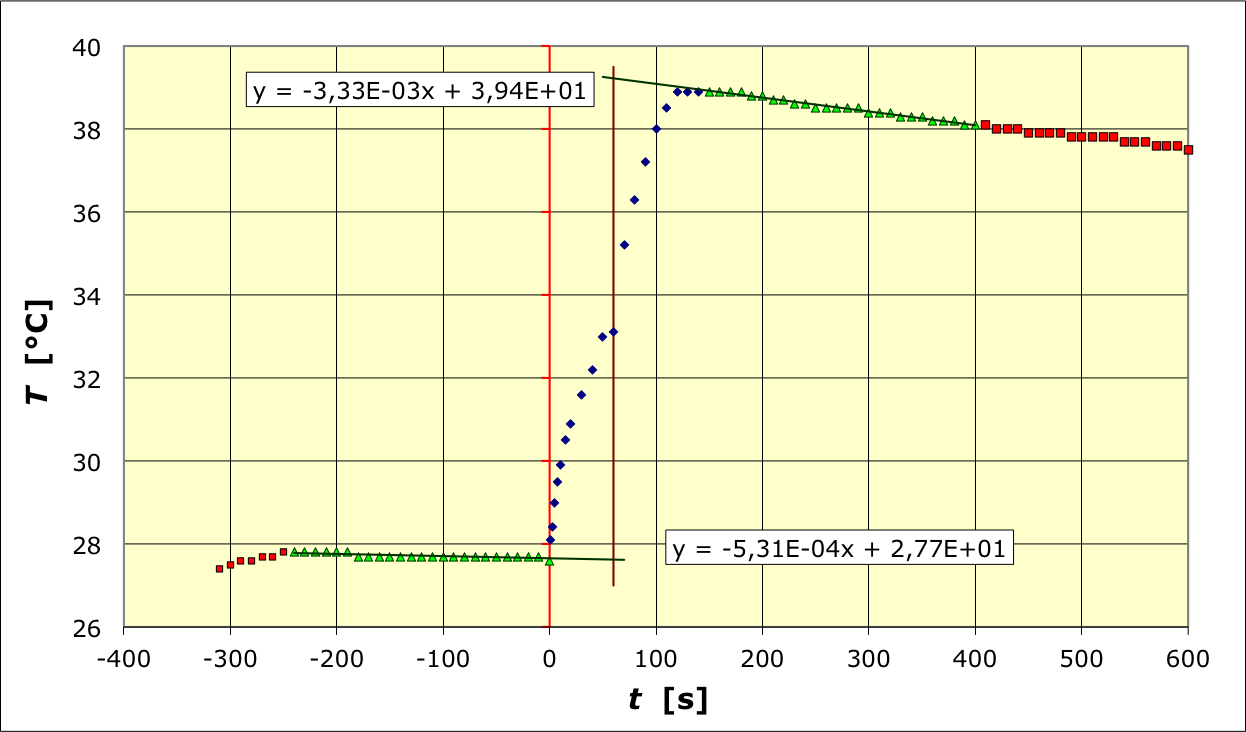
• Pour corriger les fuites thermiques, on ajuste des droites sur les
mesures avant et après chauffage ; leur prolongement jusqu'au milieu
de la durée du chauffage donne une estimation de l'effet de la
puissance moyenne des fuites (cela revient à calculer quelles
seraient les températures aux limites si le travail électrique
avait été
fourni instantanément, donc sans fuite).
On obtient pour l'eau et le calorimètre une variation
; la variation corrigée des fuites est
donc la correction est pratiquement négligeable (inférieure
aux incertitudes).
On obtient pour le fer une variation
(incertitude importante principalement à cause des fuites
thermiques lors du transvasement initial du bloc, bien qu'on procède
le plus rapidement possible, car sa température est alors très
différente de celle extérieure).
• On en déduit la capacité thermique du bloc de métal :
; ceci correspond à une valeur massique :
(tout à
fait comparable aux valeurs tabulées) et à une valeur molaire
:
hélas de précision modeste, mais compatible avec la loi de
Dulong et Petit.
◊ remarque : les étudiants n'ont pas transmis d'autres mesures pour
améliorer la précision ou pour comparer à d'autres métaux ; la
principale difficulté est l'organisation entre groupes de TP.