T.II - PREMIER PRINCIPE DE LA THERMODYNAMIQUE
Énergie interne et transfert thermique (chaleur)
☞ remarque : on se limite aux systèmes “fermés” (sans transfert de
contenu avec l'extérieur) ; on suppose en outre que les systèmes ne
sont pas en trop grand déséquilibre, afin que les notions
telles que pression et température aient une signification au moins
en chaque point.
• Les systèmes mécaniques peuvent être étudiés à l'aide du théorème
de l'énergie cinétique :
(ou de façon infinitésimale :
) ;
ceci exprime que l'augmentation d'énergie cinétique (macroscopique)
est égale au travail reçu par le système.
Certaines forces dérivent d'une énergie potentielle
,
c'est-à-dire que leur travail peut s'écrire :
. On peut alors reformuler la loi précédente sous la forme du
théorème de l'énergie mécanique :
où on n'explicite que le travail
des
forces “non conservatives”.
☞ remarque : pour les systèmes déformables, il faut prendre en
compte les travaux des forces intérieures (éventuellement
par une énergie potentielle).
• En thermodynamique, l'énergie dépend aussi de certaines propriétés
microscopiques ; la généralisation des lois précédentes nécessite de
décrire les énergies et les transferts d'énergie correspondants.
Le premier principe de la thermodynamique
consiste à postuler l'existence d’une “énergie interne” (
) ne
dépendant que de l'état du système (grandeur d’état), somme des
différentes formes d'énergies cinétiques et potentielles
emmagasinées de façon microscopique.
De la même façon qu'on appelle “travail” (
ou
) un
transfert d'énergie mécanique macroscopique, on appelle
alors “chaleur” (
ou
) un
transfert
d'énergie microscopique désordonné qui ne peut pas s’exprimer sous
une forme mécanique macroscopique (on nomme cela “transfert
thermique”).
On peut ainsi définir une “énergie totale”
:
et généraliser les lois précédentes sous la forme :
où on n'explicite que le travail
des
forces macroscopiques “non conservatives” et
extérieures (
des
forces intérieures est pris en compte par
comme
par
).
◊ remarque : lors de l'étude de la calorimétrie, on se limite
souvent aux cas où l'énergie mécanique est constante, ce qui
correspond à :
; en outre, on note souvent simplement
s'il n'est
pas nécessaire de préciser.
☞ remarque : dans le cas général,
et
ne sont
pas des fonctions d'état, c'est-à-dire que le travail ou la
chaleur reçus en passant d'un état à un autre dépendent de la façon
dont on passe de l'un à l'autre (sauf cas particuliers).
📖 exercice n° I.
Exemples de travaux
Exemples divers
• Les travaux des diverses forces exercées sur le système
s'expriment généralement sous des formes telles que :
ou
.
• Certains travaux peuvent par ailleurs être recalculés en fonction
d'autres grandeurs ; c'est par exemple le cas des travaux des forces
électriques exercées sur les porteurs de charge :
où
est la
tension électrique “traversée” par la charge infinitésimale
entre les
points
et
).
◊ remarque : selon le contexte, il faut prendre soin à ne pas
confondre tension et énergie interne (souvent notées
), potentiel
et volume (souvent notés
), charge et
chaleur (souvent notées
).
Travail des forces pressantes
• Parmi les travaux des forces exercées sur le système, les travaux
des forces pressantes doivent être pris en compte : quand un système
se dilate à pression constante, il fournit du travail au milieu
extérieur.
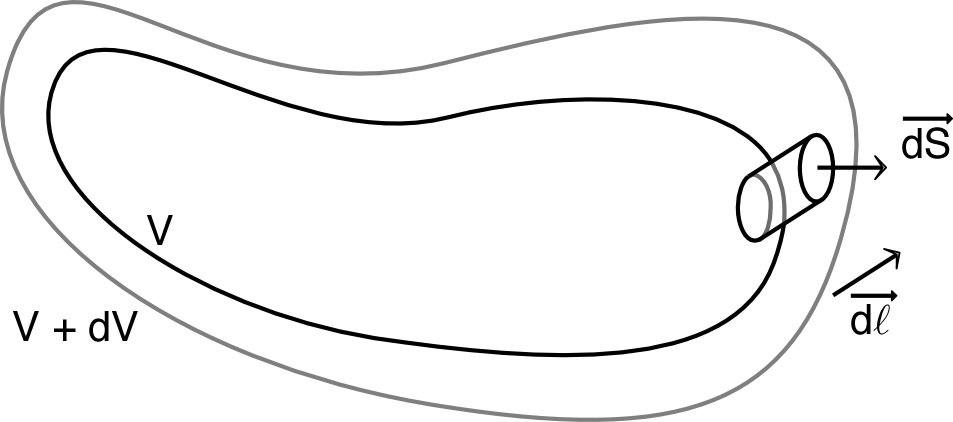
Soit
un élément de la surface (orienté dans le sens sortant) soumis à une
pression
et subissant
un déplacement
:
Le travail de la force
est :
où
est le
volume infinitésimal “balayé” par
lors du déplacement
.
Dans le cas général :
où
est la
pression frontière (valeur locale sur l’élément
limitant le
système à cet instant).
Pour un système (ou une partie) dont la pression est uniforme
(quasi-équilibre) :
où
est la variation infinitésimale du volume de l'ensemble.
◊ remarque : un système (ou une partie) est “monobare” si
est uniforme et statique partout où le volume varie (même si
la pression ailleurs ne l’est pas) ; un système est “isobare”
si
est
uniforme et statique partout.
Notion d'enthalpie
• Les expériences usuelles sont réalisées à pression “constante”
(uniforme et statique) ; les variations du volume causent un travail
des forces pressantes.
De même qu'on peut remplacer le travail des forces conservatives par
une variation d'énergie potentielle, ou le travail des forces
internes par une variation d’énergie interne, on peut définir une
nouvelle sorte d'énergie généralisée pour inclure le travail des
forces pressantes.
À pression constante (uniforme et
statique), le travail élémentaire des forces pressantes peut
s’écrire :
; on peut alors définir la grandeur d'état “enthalpie”
:
;
;
;
au lieu de
.
où le travail
correspond aux forces extérieures, non conservatives,
autres
que les forces pressantes ; le travail des forces pressantes
est ainsi automatiquement pris en compte.
◊ remarque : il ne s'agit que d'une autre façon d'exprimer le
premier principe, rien n'interdit de calculer à l'aide de l'énergie
interne
(de même que
pour l'énergie mécanique par rapport à l'énergie cinétique).
☞ remarque : réciproquement, l'enthalpie est peu pratique pour
étudier des transformations à volume constant (donc
) ; en supposant par exemple
uniforme mais
non statique :
est plus simple que :
.
◊ remarque : si la pression est statique mais non uniforme, on peut
définir l’enthalpie (grandeur extensive) par additivité :
(où ici
ne
représente pas une variation de
mais la
contribution à
du volume
élémentaire
).
Utilisation pratique du premier principe
Coefficients calorimétriques
• Pour utiliser en pratique le premier principe, il faut pouvoir
exprimer les variations de l’énergie interne (ou de l’enthalpie) en
fonction des variables thermodynamiques usuellement mesurables :
,
,
... (en
effet, contrairement à
ou
on ne
connaît généralement pas de “formules” pour
ou
).
Puisque
est une
fonction d'état, on peut exprimer sa “différentielle” (variation
élémentaire) en fonction d'un ensemble de variables indépendantes
(
,
et
sont
généralement liées par une équation d'état).
En fait, l’énergie interne est une grandeur
surtout pratique pour calculer en fonction des variables
et
, donc on
considère :
et on nomme “capacité thermique à volume constant” le coefficient
le plus fréquemment utilisé :
.
• L’avantage est que, dans les conditions usuelles, les coefficients
comme
varient peu
et peuvent être déterminés expérimentalement (par comparaison des
bilans énergétiques selon le premier principe).
Ainsi
à volume constant (et
constante) :
et donc par intégration (si on suppose
constant)
:
.
☞ remarque : on peut échauffer sans chauffer : l'augmentation
correspondant à l’échauffement
ne nécessite
pas forcément un chauffage (transfert thermique
) mais peut
être obtenu en fournissant du travail (
).
☞ remarque : ceci est lié au fait que
n’est pas une
fonction d'état et que la chaleur transférée dépend non seulement de
l'état initial et de l'état final, mais aussi de la façon dont
s'effectue la transformation ; il serait ainsi absurde d'écrire
à partir de
“dérivées partielles” d'une grandeur
.
• D’une façon analogue pour l’enthalpie, surtout
très pratique pour calculer en fonction de
et
:
; on nomme ainsi “capacité thermique à pression
constante” la quantité :
fréquemment utilisée.
À pression constante (et
constante) :
et donc par intégration (si on suppose
constant)
:
.
• Dans la mesure où les capacités thermiques
sont des grandeurs extensives, on peut les exprimer à l'aide des
capacités thermiques massiques
et
définies
par :
et
où
est la
masse du système.
On peut également utiliser les capacités
thermiques molaires
et
définies par :
et
où
est le
nombre de moles de constituants dans le système considéré.
◊ remarque : pour des raisons historiques, ces quantités sont hélas
parfois encore appelées à tort “chaleurs massiques” et
“chaleurs molaires”.
Cas des gaz parfaits
• Il existe tout de même des cas simples où la théorie cinétique
permet de trouver une expression pour les grandeurs
précédentes.
• Pour les gaz parfaits, l’énergie interne
(uniquement cinétique car ce modèle est une limite idéalisée) ne
dépend que de la température ; par exemple pour un gaz parfait
monoatomique
:
(c’est-à-dire
pour chaque “degré de liberté quadratique”).
Ceci correspond à :
et
pour un gaz parfait
monoatomique.
• De même, l’enthalpie des gaz parfaits ne
dépend que de la température :
et donc :
(relation de Mayer).
Pour un gaz parfait
monoatomique :
;
;
.
• Pour un gaz polyatomique, il faut ajouter
l’énergie cinétique de rotation :
- pour les molécules linéaires
et
(deux degrés car les rotations selon leur axe
sont négligeables) ;
- sinon
et
(trois degrés de rotation).
◊ remarque : ceci est vrai aux températures usuelles ; à très basse
température n'interviennent que les translations, puis les rotations
dans les conditions usuelles, puis les vibrations aux assez hautes
températures.
• On note généralement :
; par exemple :
pour l’air (diatomique). Pour disposer d'expressions
utilisables pour plusieurs cas (différentes valeurs de
) on peut
ainsi écrire :
.
◊ remarque : certaines relations peuvent se généraliser aux gaz
réels en ajoutant au gaz parfait un terme d'énergie potentielle
d'interaction interne ; par exemple dans l'approximation de Van der
Waals :
(où
est une
simple constante).
📖 exercice n° II.
Cas des liquides et solides
• Pour un liquide ou un solide,
quasi-incompressibles, le volume varie de façon négligeable ; on
peut donc raisonner comme si l’énergie interne ne dépendait que de
la température :
.
Pour un liquide ou un solide,
quasi-incompressibles, le travail des forces pressantes est
négligeable :
et donc
.
• Par exemple dans un solide cristallisé, en
simplifiant, on peut considérer pour chaque atome trois degrés de
liberté de vibration, associés chacun à un terme quadratique pour
et aussi
un terme quadratique pour
élastique
:
;
;
(loi de Dulong et Petit).
Exemples de calculs calorimétriques
Méthode des mélanges
• On cherche par exemple la température d'équilibre d'un mélange
étudié à pression constante (uniforme et statique) ; les transferts
de chaleur correspondent alors à des variations d'enthalpie. On
néglige par ailleurs les variations d'énergie mécanique du système.
• Soit un calorimètre “adiabatique” (parfaitement isolé
thermiquement), initialement à
, dans lequel on verse
d'eau à
; on constate que la température d'équilibre est :
.
On peut calculer la capacité thermique
du
calorimètre si on connaît la capacité thermique massique de l'eau
:
(
).
Pour le système (isolé) :
donc :
.
• On ajoute ensuite dans l'eau précédente une masse
de zinc à
.
On peut calculer la température d'équilibre
si on
connaît la capacité thermique massique du zinc :
(
).
Pour le système (isolé) :
;
.
◊ remarque : dans la mesure où n'interviennent que les variations
de température, ces calculs sont valables aussi bien pour les
températures Celsius que pour les températures Kelvin.
📖 exercices n° III et IV.
Bilan avec énergie mécanique
• On peut également étudier l'évolution d'un système comportant des
variations d'énergie mécanique.
Soit une balle de plomb de masse
, animée
d'une vitesse horizontale
, venant heurter un bloc de plomb de masse
posé sur une surface plane, horizontale et sans frottement.
Les deux sont initialement à la température ambiante.
La balle s'encastre et s'immobilise par rapport au bloc de plomb. Le
mouvement étant essentiellement horizontal, on peut négliger l'effet
de la pesanteur en première approximation (à cette vitesse elle n'a
pas le temps d'agir).
• La conservation de la quantité de mouvement (en projection sur
l'horizontale) impose :
d'où
.
Par contre :
; sous l'effet des frottements internes, une partie
importante de l'énergie mécanique (ici cinétique) est transformée en
énergie d'agitation thermique (énergie interne).
• Pour ce système pseudo-isolé mécaniquement (à part pour la
pression, mais le volume est constant) et thermiquement
(transformation trop rapide pour transférer de la chaleur vers
l’extérieur) :
.
Ceci donne :
où
est la capacité thermique massique du plomb (
)
; ainsi :
.
◊ remarque : il est très compliqué de traiter un tel
problème en considérant séparément la balle et le bloc, car
l’interaction par frottements est plus compliquée qu'il n'y parait ;
la notion d'énergie interne, ou d’enthalpie, sert justement à éviter
de se poser ce type de questions :
.
📖 exercice n° V.