|
☞ remarque : on suppose que la fuite est
assez petite pour que la distribution statistique des
vitesses soit toujours conforme au facteur de
Boltzmann
, sinon tous les calculs basés sur les moyennes seraient
modifiés.
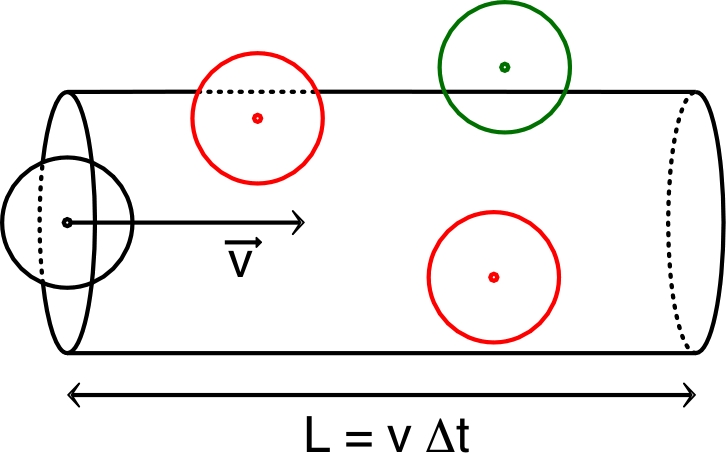
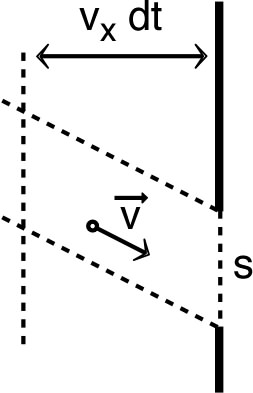
• Les atomes de vitesse
qui viennent de la gauche et
atteignent
pendant une durée
sont ceux qui sont distants d'au plus
. Ceci est indépendant des autres composantes
du mouvement ; on peut donc raisonner comme si tous
les constituants se déplaçaient selon
.
• Leur nombre est en moyenne :
. Par ailleurs, d'après la symétrie,
calculée sur les vitesses positives correspond
à
calculée sur l'ensemble des vitesses.
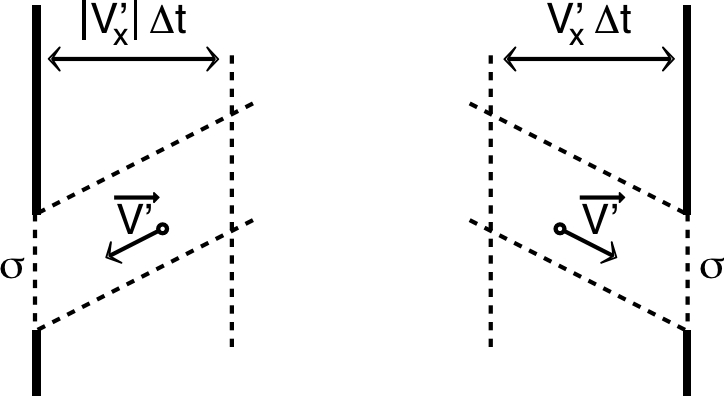
• De même, les atomes de vitesse
venant de la droite et atteignant
pendant une durée
sont ceux qui sont distants d'au plus
. |
|
|
• Leur nombre est en moyenne :
. Par ailleurs, d'après le facteur de Boltzmann, la
moyenne des vitesses ne dépend que de la température, donc
elle est la même des deux côtés.
• Au total (compte tenu de
, noté
)
:
.
• Puisque
est constant :
; on obtient donc :
en notant
. On en déduit par intégration, compte tenu des
conditions initiales :
.
◊ remarque : on doit retrouver qu'à la limite le gaz est
réparti uniformément dans les deux récipients.
• D'après la proportionnalité dans la loi des gaz parfaits
:
. Par suite, on obtient
pour
.
• Pour calculer
on ne
connaît pas
mais on peut en estimer l'ordre de grandeur,
comparable à la vitesse quadratique moyenne :
; ceci donne :
et finalement :
.
◊ remarque : le calcul complet de la moyenne (pondérée par
le facteur de Boltzmann correspondant) donne :
avec :
;
;
ainsi :
(ce qui
est bien de l'ordre de grandeur envisagé) ; cela donne plus
précisément :
et finalement :
. |