• Calculer la variation du niveau pour une variation de la pression atmosphérique ; en déduire le gain en précision par rapport au baromètre ordinaire.
|
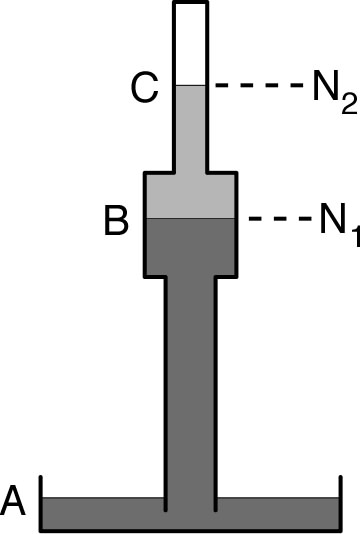
• Le tube barométrique comporte un renflement
de
section
surmonté d’un tube
de
section
. Le mercure monte jusqu’au niveau
,
environ au milieu de
; il
est surmonté par de la glycérine dont la surface libre est
au niveau
.
L’espace au dessus de
est
pratiquement vide (la pression de vapeur de la glycérine est
négligeable). • Calculer la variation du niveau pour une variation de la pression atmosphérique ; en déduire le gain en précision par rapport au baromètre ordinaire. |
 |
| données : |
;
;
; masses volumiques : mercure : ; glycérine : . |
à ; à ; à .• Montrer que dans le domaine de à cette f.e.m. peut être représentée par une expression de la forme : et déterminer les coefficients et .
à ; à ; à .• Montrer que cette résistance peut être représentée empiriquement par une expression de la forme : (déterminer les coefficients et ).
| |
données : |
;
; ; . |
|
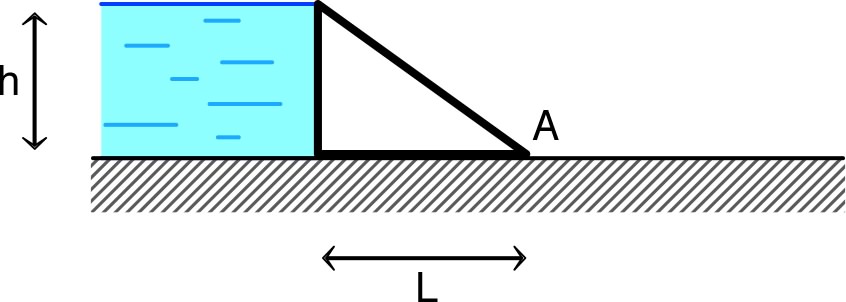
• Un mur de barrage, retenu uniquement par son contact avec
le sol, a le profil ci-contre (en coupe), avec une
hauteur
, une largeur
et
une longueur
. • La densité du matériau de construction est ; le “coefficient de frottement solide” au sol est (valeur maximum du rapport entre le frottement et la réaction normale du sol à la limite de glissement). |
 |
(dilatation isobare) ; (compressibilité isotherme) ;
augmentation thermique de à volume constant.
(dilatation isobare) ; (compressibilité isotherme) ;
augmentation thermique de à volume constant.