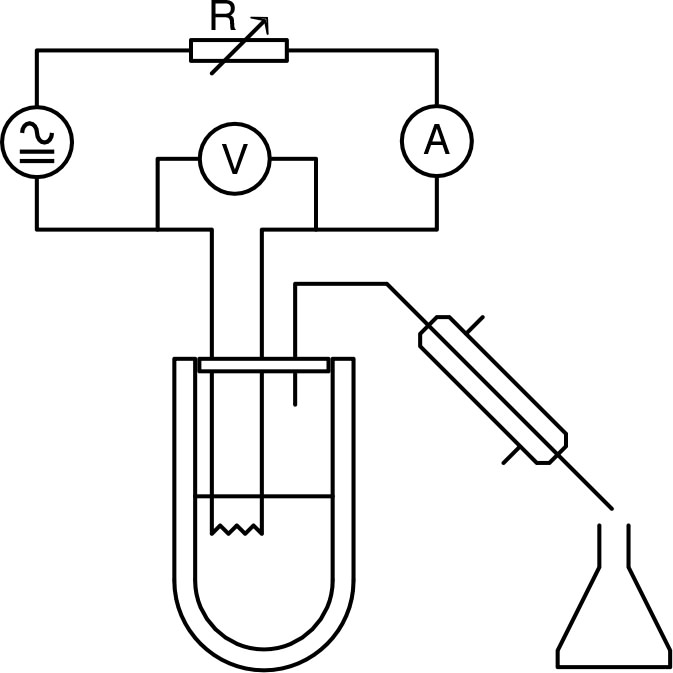
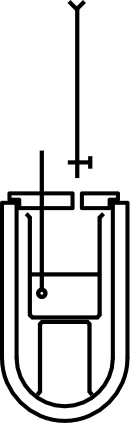
• Dans un calorimètre de capacité
calorifique
négligeable (vase Dewar), on place un volume
de
solution de
à la concentration
,
puis on la neutralise par une solution de
à la concentration
.
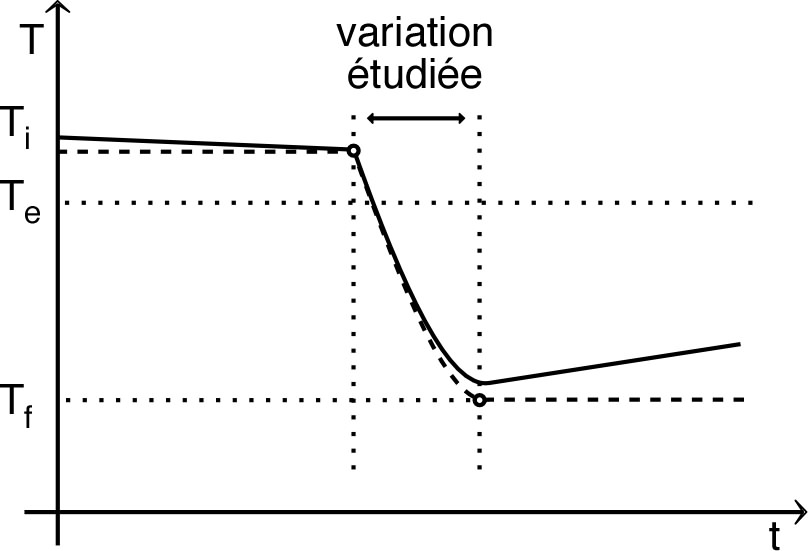
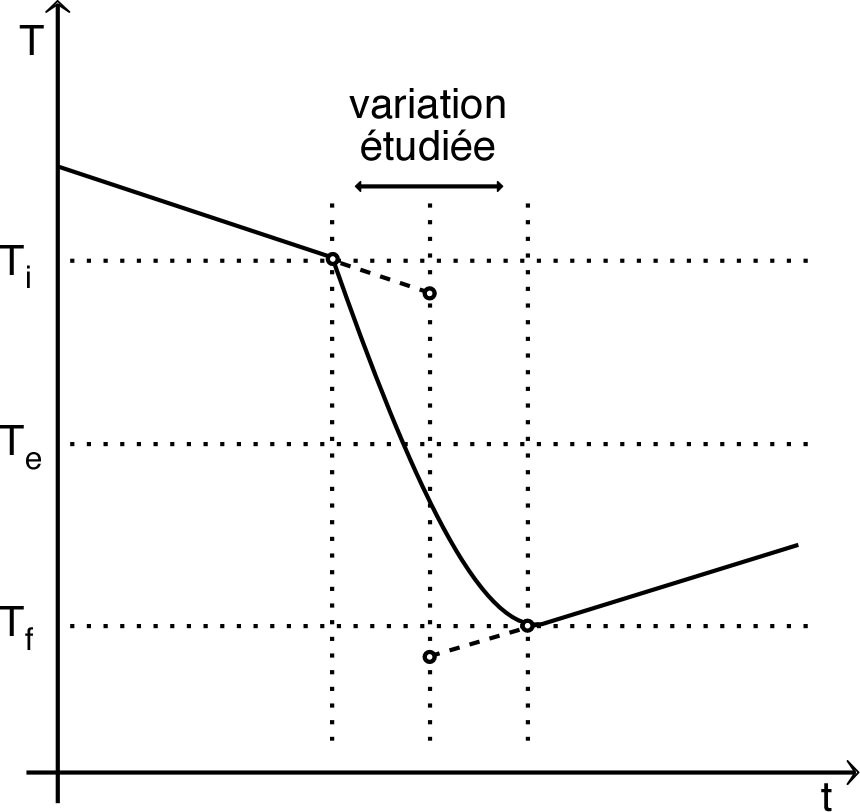
• Le système étant thermiquement “isolé” à pression
constante :
(avec
)
et on peut donc en déduire
par mesure la température en fonction du volume
de
solution de
(le signe
devant
correspond au fait que la neutralisation, exothermique, est
la réaction inverse de l’autoprotolyse). |
|
|